AACRニュース:米国癌学会AACR 2023のハイライト
2023 年 4 月 24 日
世界中の科学者は、がんの成長、分裂、転移を引き起こす分子メカニズムを解明するために熱心に研究に取り組んでおり、患者の寿命を延ばし、これらの病気の一部を治す可能性さえある、より良い治療法を開発するのに役立てています。
2023 年の米国癌学会 (AACR) 年次総会ではこれらの科学者の努力が発表されました。ご存知のように、膵臓がんは最も治療が難しいがんの 1 つですが、科学がこの致命的な悪性腫瘍をより効果的に治療できるものに変えようとしていることが明らかになりました。ここでは米国癌学会2023のハイライトをいくつか紹介します。
■KRASを倒す
2021 年に KRAS-G12C 変異を有する非小細胞肺がんを治療するためのソトラシブ( 一般名Sotorasib、商品名Lumakras) が承認されたことで、KRAS は創薬不可能な発がん遺伝子から創薬可能な治療標的に変わりました。この医薬品の承認は、がんの研究と治療に一夜にしてセンセーションを巻き起こしました。 KRAS 変異を直接標的とすることで、全ヒトがんの約 4 分の 1 に対する効果的な治療法を研究するための準備が整いましたが、その興奮によって、より冷静な現実が見えなくなることがあってはいけません。ソトラシブとそれに続く KRAS 標的薬剤は、数十年にわたる骨の折れる基礎および応用がん研究の成果だからです。
免疫療法と標的療法の最近の進歩により、多くの患者の転帰が大幅に改善されてきました。しかし、これらの進歩は RAS 変異腫瘍を有する患者の転帰改善にはまだ限定的であると、ニューヨーク大学ランゴンヘルスの生化学および分子薬理学の教授であるダフナ・バー・サギ博士(Dafna Bar-Sagi, Ph.D.)は注意を促します。しかし、KRASの状況は、RAS を直接標的とする治療法の出現と免疫介入技術の改善により劇的に変化してきているのも事実です。
G12C は、RAS 駆動型腫瘍で最も一般的な変異であり、肺がんでよく見られます。現在開発中の対立遺伝子特異的阻害剤の標的である膵臓がんやその他のがんには、さまざまな RAS 対立遺伝子変異(膵臓がんに多いいのはG12D, G12Vの変異)があります。最もエキサイティングな開発の 1 つは、対立遺伝子にとらわれず、構成的に活性なすべての RAS を標的とする汎 RAS 阻害剤です。低分子阻害剤に加えて、研究者は養子細胞療法やタンパク質の変異型に対するワクチンなど、KRAS 変異腫瘍に向けられた他の治療法の開発にも取り組んでいます。
これらのアプローチは、多くの固形腫瘍の適応症に対する新しい個別化医療戦略を表しており、それらが RAS 腫瘍に対して機能することは、この分野における大きな進歩となるでしょう。実際、抗 KRAS 療法は、最も致死率の高いいくつかの癌の治療に有望です。しかし、科学者たちは、RAS だけをターゲットにするだけではおそらく十分ではないことを学びつつあります。これは、まだ科学者たちの発見の栄光に満足している時ではないことを意味します。腫瘍がこれらの治療法に対してなぜ、どのように耐性を持つようになるのかを研究し、その耐性を克服するための新しいアプローチを設計することが依然として重要な研究テーマだからです。
UCSF ヘレン ディラー ファミリー総合がんセンター(サンフランシスコ) の フランク・マコーミック博士(McCormick, Ph.D., F.R.S.)は、「RASを倒すための競争(The Race to Kill RAS)」の歴史と進行中の取り組みに関する重要な情報を追加しました。 マコーミック博士は、これらの目標に対処するために現在評価中の治療アプローチのいくつかを強調しました。彼は、研究中の KRAS 阻害剤であるBBO-8520 からの有望な結果を共有しました。 KRAS G12C の不活性型に結合するソトラシブやアダグラシブとは異なり、この化合物はKRASの活性型も標的とします。この機能により、BBO-8520 は RAS がアクティブ状態から非アクティブ状態(非活性型)に切り替わるのを待つ必要がないため、ソトラシブやアダグラシブよりも迅速に RAS を阻害すると マコーミック博士は説明しました。
同じく発表者であるダナファーバーがん研究所(ボストン)のパシ・ジャンヌ医学博士( Pasi Jänne, M.D.)も、活性型 KRAS の阻害に関心を持っています。彼は、複数の KRAS 変異体の活性型を標的とする治験中の 汎KRAS 阻害剤の有効性を示す有望な前臨床および臨床データを共有しました。彼はまた、KRAS阻害剤を免疫チェックポイント阻害剤を含む追加の治療法と組み合わせる可能性についても議論しました。
研究者は、KRAS 変異がんを標的とするさまざまな方法で免疫系を利用することも検討しています。ペンシルバニア大学 (フィラデルフィア) のペレルマン医学部のベアトリス・カレーノ 博士(Beatriz Carreno)は、治験用ワクチンを投与された患者は、KRAS 変異がんに見られるネオアンチゲンに対して T 細胞応答を示したと報告しました。さらに、これらのネオアンチゲンを認識するように設計された T 細胞は、患者由来のがん細胞株を効果的に殺し、マウスモデルで腫瘍の退縮をもたらしました。
膵臓がんのKRAS変異分布図
G12D 39.2%, G12V 32.5%, G12R 17.1%, G12C 1.7%
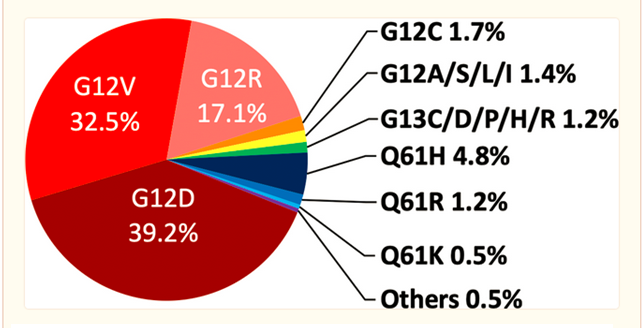
SOURCE: Ji Luo, PhD. KRAS mutation in Pancreatic Cancer. Semin Oncol. 2021 Feb; 48(1): 10–18.
■がんの科学と医学の最前線を前進させる
メモリアル スローン ケタリングがんセンター (ニューヨーク) の医学部長であるデブ・シュラグ医学博士(Deb Schrag, M.D., M.P.H.)は、複数のがんの早期発見 検査 (MCED)の可能性を含む、がん検診を変革する新しいがんスクリーニング技術の拡大の可能性と課題について議論しました。30 以上の企業によって開発された MCED テストは、現在、さまざまな開発段階とテスト段階にあります。いくつかの初期の研究は心強いものですが、シュラグ医学博士は、MCED 検査ががん特異的死亡率 (すべてのがん検診の主な目標) を減らすかどうかを評価するには、臨床的有用性研究が必要であると述べました。
編集注:多癌早期発見検査 (MCED) には、単一の血液サンプルから複数の種類の癌を検出できる可能性があります。血液サンプルは、がん細胞に由来する特定の DNA またはタンパク質の断片について検査されます。これらが見つかった場合、その人ががんを患っていることを示す可能性があり、がんがどの臓器から発生したかがわかる可能性もあります。一部の MCED 検査は、体のどこかにがんがある可能性を検査するだけなので、人が陽性反応を示した場合、異常な DNA やタンパク質が体のどこから来たのかを解明するには、画像検査などの他の検査が必要になります。
ワシントン大学医学部 (ミズーリ州セントルイス) の腫瘍学部門の医学教授であるデビッド・デナルド博士(David DeNardo, Ph.D.)は、がんの全身への影響を調節するなど、抗がん免疫を刺激する新たな治療戦略、免疫系と腫瘍微小環境の標的化について概説しました。免疫に基づく治療は進歩し続けていますが、すべての患者が免疫療法の恩恵を受けるわけではありません。課題は、反応する可能性が高い患者を特定し、反応がまだ持続していない患者の持続性を高め、免疫系を活用して免疫療法にまだ反応していない患者やがんの種類に利益をもたらす方法を研究し理解することです。
オレゴン健康科学大学ナイトがん研究所 (ポートランド) の細胞、発生、およびがん生物学の教授であるテレサ・A・ジンマーズ博士(Teresa A. Zimmers, Ph.D.) は、悪液質の複雑さとがん転帰への影響に関する重要な新しい洞察を説明しました。 ジンマーズ博士は、悪液質に対する実証済みの治療オプションを開発する必要性が非常に大きいと述べています。
■がん研究生涯功労賞
キメラ抗原受容体 (CAR) T 細胞は、がん治療の議論に治癒という言葉を追加しました。しかし、CAR T 細胞が治療法として想定されることはありませんでした。癌研究における生涯功績に対して今年の AACR 賞を受賞した ペンシルバニア大学ペレルマン医学部のカール・H・ジューン医学博士によるCAR T細胞の開発に関する受賞講演の中で、マウスモデルの有望なブレークスルーからモダリティ初のCAR T細胞療法への予想外の移行について話しました。
血液がんを治療するための CAR T 細胞療法の開発は、比較的一般的な疾患を治療するための薬剤に焦点を当てるという従来の医薬品開発パラダイムもひっくり返しました。従来のアプローチでは、患者を 1 人ずつ、または一度に数千人ずつ開発して治療することを業界に奨励することはできません。細胞療法および遺伝子療法は、より効果的ですが設計、製造、提供がより複雑で、超個別化アプローチにより個々の患者に固有の疾患を治療することが可能になり、実用的になったため、研究者、業界、規制当局、および臨床医が希少疾患と正面から立ち向かわざるを得なくなりました。
■早期発見
ジョンズ・ホプキンス医学およびシドニー・キンメル総合がんセンター(メリーランド州ボルチモア) のエラナ・ジュディス・ファーティグ博士(Elana Judith Fertig , Ph.D.) は、膵臓がんの発生、つまり膵臓がん発生時の腫瘍細胞と微小環境との相互作用を研究するための空間マルチオミクス アプローチについて説明しました。
新しい単一細胞および空間分子プロファイリング技術により、進行性膵臓がんの微小環境の細胞および分子組成の前例のない特性評価が可能になりました。これには、免疫抑制に関連する細胞の高密度組成が含まれます。これらの技術と機械学習および数学的モデリングの融合により、膵臓がんの免疫抑制を阻止するための候補治療法を特定できる可能性がもたらされます。
イルミナ社の フィリップ・G・フェボ医学博士(Phillip G. Febbo, M.D.)は、社会レベルでのがんの早期発見の複雑さと、新しい多がん早期発見検査 (MCED) を含む検査への公平なアクセスを通じてがんの転帰を改善する可能性について取り上げました。
国立衛生研究所(NIH)の「 All of Us Research Program」 のチーフ エンゲージメント オフィサーであるカリエム ワトソン博士 (D.H.Sc.、M.S.、M.P.H.) は、患者の転帰を改善するための鍵として、がんの早期発見戦略におけるコミュニティの関与の重要性を強調しました。ワトソン博士の研究は、コミュニティの関与が、健康的な行動の重要性に関するコミュニティの知識を増やし、研究への信頼を築き、研究のデザインと倫理を改善することにより、がんの健康格差を緩和するのに役立つことを実証しています。生物医学研究で歴史的に過小評価されてきた集団に重点を置いた医学研究へのアクセスと意識の向上は、早期発見のための革新的で新しい画期的な治療法の範囲を拡大し、がんの転帰を改善することも示されています。
他のプレゼンターが概説したように、MCED はリスクをもたらす可能性があります。 MCED 検査の大きな可能性にもかかわらず、MCED 検査についてはまだ多くが不明であり、次のような多くの未解決の問題が残っています。
・彼らの将来の癌のリスクは増加しますか?
・MCED 検査が、がん転帰における人種的、民族的、社会経済的格差を悪化させる可能性はありますか?
これらはほんの一例です。明らかなことは、最も重要な問題は、これらの検査が実際にがんによる死亡を減らすかどうかということであり、それががん検診の最終的な目標であるということです。それらの利点を最大化し、潜在的な害を最小限に抑える最善の方法を理解するには、さらなる研究が必要です.
■膵臓がん: 将来のプレシジョン メディシン試験の情報提供
ジェニファー・J・ノックス医学博士(大学医療ネットワーク、プリンセス・マーガレットがんセンター、カナダ、オンタリオ州トロント)は、膵臓がんにおける最近のブレークスルーと失敗した試験をレビューしました。彼女は驚くべき統計を見つけました。 2,600 人の患者を登録した 6 つの試験では、改善された治療法が正しい方向に効果的に針を動かせませんでした。
科学者たちは、どの患者がゲムシタビン/ナブ-パクリタキセルとFOLFIRINOXの組み合わせから最も恩恵を受けるかという問題にまだ取り組んでいます。しかし、彼らは進歩しています。たとえば、COMPASS 試験では、RNA シグネチャが化学療法に対する反応と相関していることがわかりました。 ノックス博士は、より小さなコホート、より強力な仮説、および腫瘍自体のより深い特徴付けを伴う試験を設計する時が来たと考えています。たとえば、PASS-01 試験には、患者の詳細なゲノム プロファイリング情報が含まれています。また、新しい PARP 阻害剤や KRAS-G12D を標的とする薬剤など、有望な薬剤が期待されています。
ミシガン大学医学部アン アーバー校の免疫外科教授であるマリーナ パスカ ディ マリアーノ博士(Marina Pasca Di Magliano,Ph.D.)は、患者の異質性をよりよく理解するために免疫プロファイリングを使用すること、および研究者が検出可能な腫瘍の変化をどのように血中で見つけることができるかについて話しました。
■新しい免疫療法の併用試験
転移性ステージ IV の膵臓癌に対する FOLFIRINOX への Salmonella-IL2 の追加に関する研究では、FOLFIRNOX のみを投与された歴史的対照群および部位特異的対照群と比較して、この併用により生存期間の中央値がほぼ 2 倍になることがわかりました。これは、より大規模なピボタル第 III 相多施設試験が必要であることを強く示しています。この研究の背後にあるグループには、ペトル・カヴァン、医学博士(Petr Kavan、M.D.、Ph.D.)など が含まれています。
ジョンズ・ホプキンスで作業が進行中の研究で切除された膵臓癌におけるイピリムマブ/ニボルマブと組み合わせた最初のヒト変異体KRASロングペプチドワクチンの安全性と免疫原性もレビューされ、膵臓腺癌の手術後の変異体KRASワクチンと免疫療法の予備データもレビューされました。膵臓がんに対する個別化された mRNA ネオアンチゲン ワクチンに関するプレゼンテーションは、メモリアル スローン ケタリングがんセンターのヴィノッド・バラチャンドラン 医学博士(Vinod Balachandran, M.D.)によっても行われました。
■エリザベス・ジャフィー医学博士に敬意を表して
AACR は、著名な膵臓がん研究者であり、AACR アカデミーのフェローで AACR の元会長でもあるエリザベス M. ジャフィー医学博士(Elizabeth M.Jaffee, M.D.)に、がん研究におけるリーダーシップと並外れた功績に対して 2023 年 AACR-マーガレット フォティ賞が授与されました。
ジャフィー博士は革新的な研究の先頭に立ち、いくつかの免疫療法の開発と臨床評価をもたらしました。特に、彼女は、免疫刺激性サイトカインである顆粒球マクロファージコロニー刺激因子(GM-CSF)を分泌するように操作された膵臓癌細胞を送達し、それによって抗腫瘍免疫の活性化を促進する、膵臓癌用の同種異系 GVAX 癌ワクチンの試験と開発に貢献しました。ジャフィー博士は、GVAX と CRS-207 ワクチンの併用も検討しています。
彼女の研究は、膵臓がんの発症と進行のバイオマーカーを定義するためのゲノムおよびプロテオミクス技術の活用にも焦点を当てています。これらの研究により、アネキシン A2 が膵臓癌転移の潜在的な調節因子として同定されました。ジャフィー博士の現在進行中の研究は、新しい技術を利用して、膵臓癌の腫瘍細胞、単球、および間質細胞の間に存在する複雑なシグナル伝達経路を明らかにし、これらの通信をバイパスして抗腫瘍免疫応答を増強する新しい方法を開発することを目的としています。
Source: Let's Win -sharing science solutions for pancreatic cancer, Lustgarten Foundation
ーーーーーーーーーーーーーーーーーーーーーーーーーーー
<免責事項>この医療記事は、海外の最新のがん研究、臨床試験などを紹介する目的で書かれています。特定の治療法や薬の使用を推奨するものではありません。ご自身の病状については、担当医とよく話し合ってください。このウェブサイトの情報を利用して生じた結果についてPanCANJapanは一切責任を負うことができませんのでご了承ください。