(祝)ラロトレクチニブが膵臓がんに承認される
2021年3月23日
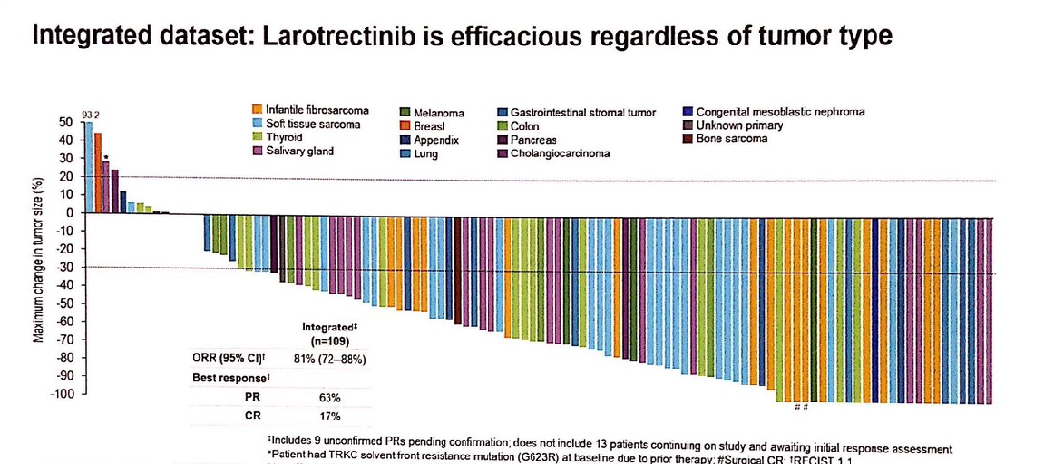
バイエル薬品は、本日「NTRK陽性の固形がん」を対象疾患とする新規TRK阻害薬ラロトレクチニブ(商品名ヴァイトラックビ)が厚労省に承認されたと発表しました。ラロトレクチニブは、膵臓がん、胆管がん、軟部肉腫、乳児型線維肉腫、消化管間質腫瘍、唾液腺がん、甲状腺がん、肺がん、悪性黒色腫、大腸がんなど20 以上の組織型にわたる固形がんで承認されました。
独バイエルのスコット・フィールズ氏は、日本での承認を受けて、「がんの治療薬はこれまで主に発生部位ごとに承認されてきたが、ラロトレクチニブはがんの発生部位にかかわらず、TRK融合を有するがん患者さんを対象として承認された」と説明しました。「NTRK融合遺伝子を有する成人および小児がん患者さんの治療に特化して開発されたラロトレクチニブは、がん腫や年齢によらず治療成績を大幅に改善する可能性を持ちます。」とコメントしました。
何らかの原因でNTRK遺伝子とその他の遺伝子が転座し接合されることがあり、その結果、融合してできる異常な遺伝子は「NTRK融合遺伝子」と呼ばれます。NTRK融合遺伝子から転写・翻訳して合成される異常なTRK融合タンパクが発がんの原因になり、がん細胞の増殖を促進すると言われています。
がん遺伝子パネル検査をもとに選択できる膵臓がんに承認された薬剤は、これで4剤となりました。MSIーH/TMBーH 患者を対象としたチェックポイント阻害剤ペンブロリズマブに始まり、TRK融合遺伝子阻害薬エントレクチニブ、BRCA遺伝子阻害剤オラパリブ、そして今回のTRK融合遺伝子阻害剤ラロトレクチ二ブです。
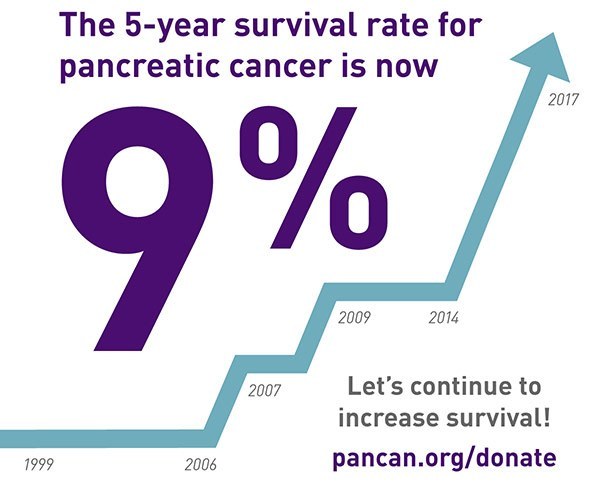
パンキャンジャパンでは、4月の『膵臓がんナショナルアドボカシーデー活動』において、膵臓がん患者が診断時にこれらの膵臓がんで承認された薬剤を選択できるよう、それに必要ながん遺伝子パネル検査がアメリカのように診断時に受けられるよう厚労省に要望書を提出します。その大きな理由は、アメリカのように患者が膵臓がんの診断時にがん遺伝子パネル検査を受けることができれば、25%以上の膵臓がん患者にアクショナブルな遺伝子変異が見つかり、対応する薬剤を使って治療を受けることができます。
アメリカでは費用対効果がよいのは、診断時にパネル検査を受け、その結果をもとにして治療を選択することだとしています。しかし、日本では、いまのままだと医師が膵臓がんの診断時にすぐに患者にパネル検査を受けさせることができないために、これらの新しく承認された薬剤をすぐに検討することができません。そして、日本では標準治療が終了するまで待たないとパネル検査が受けられないこと、また、組織生検を送ってから2か月待たないと、エキスパートパネルからの審査結果が戻ってこないこと、さらに新薬につながる遺伝子変異陽性が見つかってたとしても、難治な膵臓がん患者の体力も落ち、奏功する新薬を使うことができないことになりかねないことなど、ゲノム医療の入口、出口に問題が山積しています。膵臓がん患者のおかれているこのような現状を改善し、膵臓がん患者を救うために、ぜひ要望書に署名して、パンキャンジャパンの要望活動を支援してください。ネット署名はこちらから ☞ https://www.pancan.jp/index.php?option=com_content&view=article&id=433&Itemid=800