海外ニュース:Gem耐性進行膵癌にイリノテカンリポゾーム(オニバイド)多剤併用療法(セコンドライン)
2016年5月24日
Merrimack社は、イリノテカンリポゾーム注射液(商品名:オニバイドOnivyde)+フルオロユラシル (5-FU)+ロイコボリン併用療法が2016年版NCCN診療ガイドライン(2016 NCCN Clinical Practice Guidelines in Oncology)に、ゲムシタビン耐性の進行膵がん患者さんのセコンドライン治療として表記されたと発表した。この併用療法は、エビデンスレベルが一番高い「カテゴリー1」が与えられている。「ゲムシタビンを使用した治療に耐性ができた患者のための唯一のFDA承認を受けた治療法として、治療法が限られた患者のアンメットニーズに答えるものである」とMerrimack社のスポークスマンは語った。
我が国の膵臓がん患者は、この国際標準治療薬が使えない。アメリカでは、すでにこの最新の医薬品を使った併用療法に臨床試験が進められているが、日本は未承認であるがために国際共同治験に入れない可能性がでてきている。日本のドラッグラグ問題は、いまだに解決しない、深刻な課題である。膵臓がん患者支援団体パンキャンジャパンではドラッグラグ問題解決にむけた署名活動を続けているが、この医薬品の早期承認を目指した活動を活発化したい。ゲムシタビンに耐性ができて、次の薬を探している進行膵がん患者には時間的余裕がない。待てない患者のために、日本の製薬企業には、膵臓がんの領域で拡大治験にも取組んでほしい。
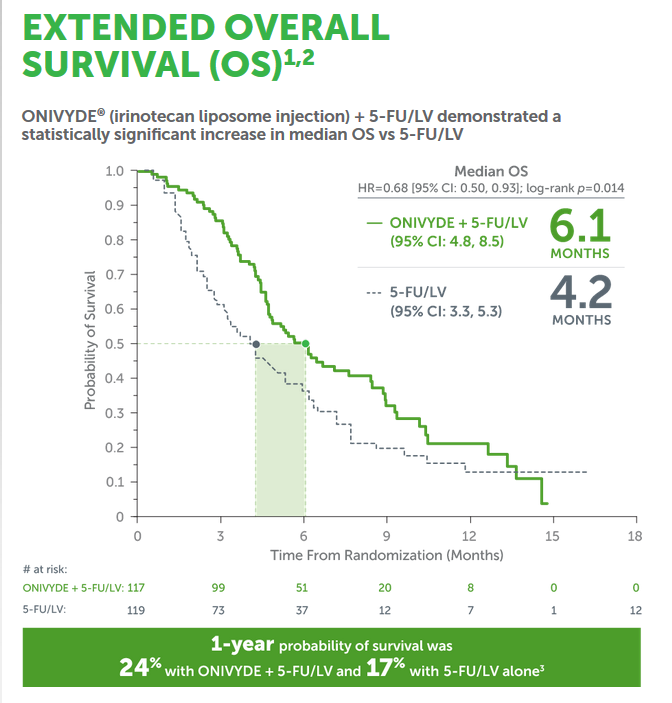
参考資料: http://global.onclive.com/web-exclusives/second-line-liposomal-irinotecan-added-to-nccn-guideline#sthash.PTtXXJow.dpuf