AACR ニュース:膵臓がん特別会議委員長とのインタビュー
AACR VIRTUAL SPECIAL CONFERENCE:PANCREATIC CANCER
September 29-30, 2020
AACR Virtual Special Conference
2020年9月25日
著者 カレン・オルセン PhD
AACRオンライン膵臓癌特別会議:2020年9月29〜30日
会議の共同議長
・ダフナバーサギ、ニューヨーク大学ランゴーン医療センター、ニューヨーク州ニューヨーク
・エリザベスジャフィー、ジョンズホプキンスシドニーキンメル総合がんセンター、メリーランド州ボルチモア
・ベン・Z・スタンガー、ペンシルベニア大学エイブラムソンがんセンター、ペンシルベニア州フィラデルフィア
・ブライアンウォルピン、ダナファーバー癌研究所、マサチューセッツ州ボストン
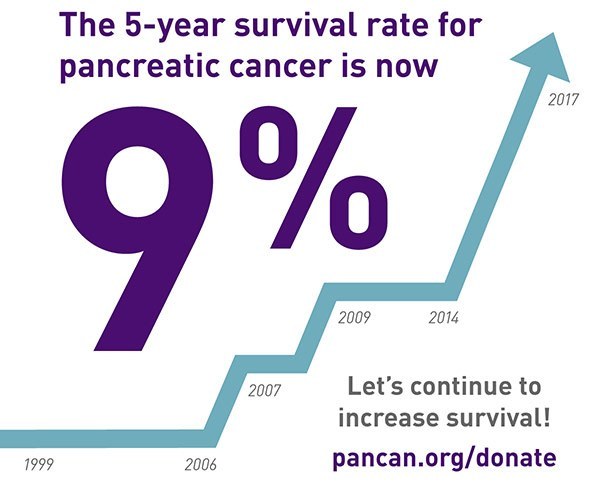
膵臓癌は、今年だけで米国で約45,750人の死亡を占め、2030年までに癌による死亡の3番目の主要な原因になる準備ができています。膵臓癌に関する仮想AACR特別会議は、最先端の発見と有望なものの多くを紹介します。膵臓がんの理解と治療の進歩。全体会議のトピックは、基礎研究の発見から証拠に基づく臨床試験まで、膵臓がん研究のすべての側面をカバーし、世界的に有名な専門家を招集して最新の進歩について話し合います。
膵臓癌の困難な予後に動機付けられて、膵臓癌分野での実質的な研究は、新しい治療戦略とともに、疾患の生物学的推進力のより良い理解をもたらしました。この分野の重要な進歩に遅れないようにするために、AACRは毎年膵臓癌に特化した特別会議を開催しています。 2012年に隔年シリーズとして始まったこの特別会議は、昨年年次会議に移行しました。今年の会議は、9月29日から30日に開催されます。米国癌学会特別膵癌会議2020の共同議長であるシドニーキンメル総合がんセンターのAACR元会長エリザベスM.ジャフィー医学博士、FAACR、ダフナ・バー・サギ博士、FAACR、ニューヨーク大学ランゴーン医療センター、ダナファーバー癌研究所のブライアン・ウォルピン医学博士、MPH、さらにペンシルベニア大学エイブラムソンがんセンターのベン・スタンガー医学博士に伺いました。
続きを読む...